擾素;純化干擾素蛋白;無標籤干擾素;融合標籤干擾素;干擾素蛋白質量評價
一、干擾素的類別與基礎結構特徵
干擾素(interferon,IFN)是一類具有典型結構模式的小分子蛋白,在哺乳動物中廣泛表達,其最顯著的特徵是以摺疊緊湊的 α 螺旋結構或二聚體結構實現分子穩定性。按照分子結構、序列特徵以及受體識別方式的差異,干擾素主要分為 I 類、II 類和 III 類三大類。三類干擾素均屬於分子量相對較小、摺疊敏感度較高的蛋白質,因此其結構構象在文獻中經常被作為討論重點。
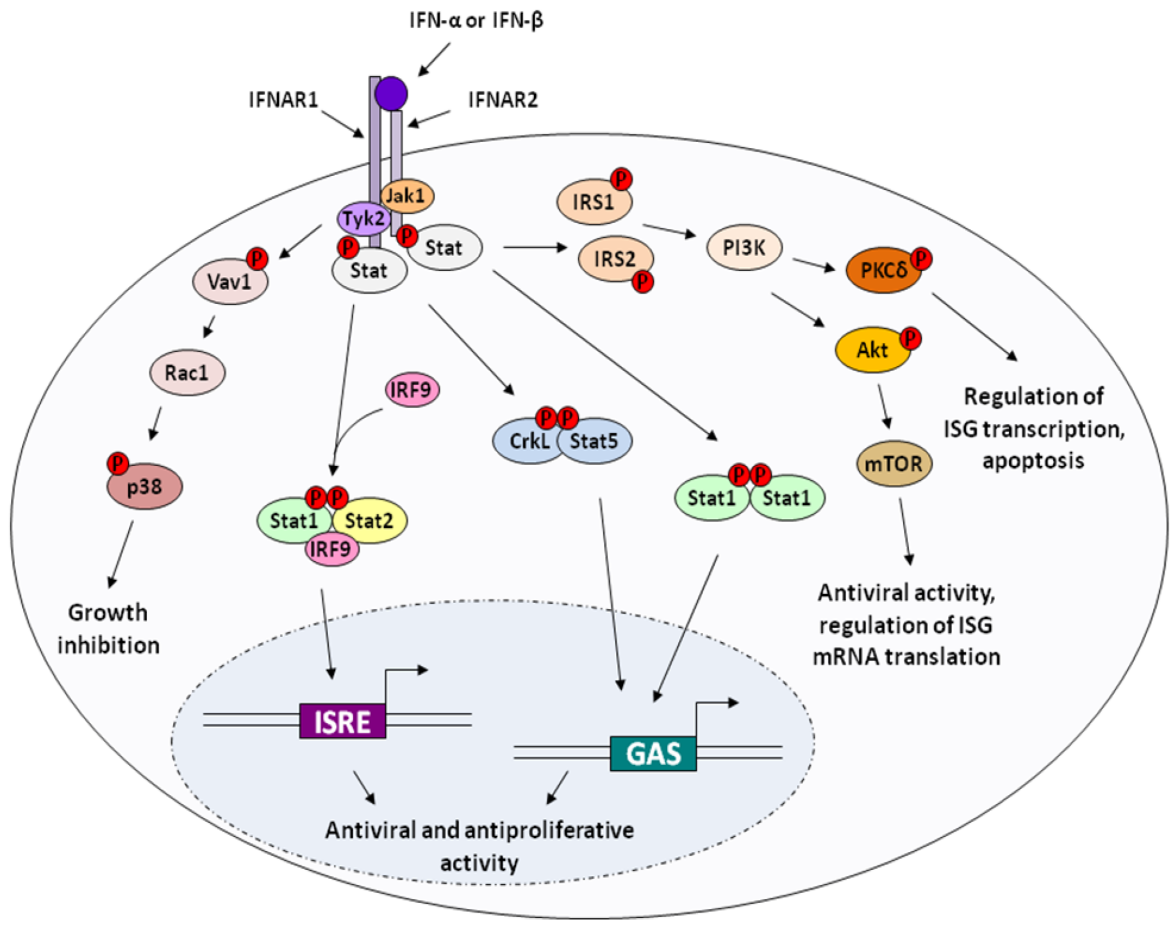
I 類干擾素包括大量 IFN-α 亞型以及 IFN-β。儘管 IFN-α 的亞型眾多,但其整體摺疊模式保持高度一致,一般由幾條 α 螺旋組成緊湊的四螺旋束結構。該結構不僅賦予其較高的摺疊穩定性,也決定了其在空間上適於與 IFNAR1 和 IFNAR2 接觸。IFN-β 則在序列和部分修飾位點上與 IFN-α 存在一定差異,但整體仍屬於 I 類干擾素典型的 α 螺旋蛋白架構。此類干擾素多以單體形式存在,其分子量集中在 20 kDa 左右,是細胞因子領域中結構相對明確的一類小分子蛋白。
II 類干擾素僅包括 IFN-γ,其最突出的結構特徵是穩定的二聚體構象。IFN-γ 以二聚體作為天然狀態,這一構象對其維持結構功能完整性具有重要意義。二聚體通常由兩個相同亞基組成,總分子量約 34 kDa。亞基之間的非共價相互作用形成穩定的界面,使整個體系呈現更為規則的空間構型。這種二聚體架構也使其在與 IFNGR1 和 IFNGR2 結合時能形成較大、幾何排列較為明確的多元複合體。
III 類干擾素,即 IFN-λ,結構模式與 I 類干擾素不同,其分子更接近 IL-10 家族的摺疊方式,呈現相對開放的 α-螺旋結構佈局。IFN-λ 的序列保守區域集中在與受體 IFNLR1 和 IL10RB 接觸的界面,受體結合所需的空間構象因此較為明確,文獻中常在此基礎上探討其穩定性與摺疊模式。由於結構與其他干擾素差異較大,IFN-λ 在科研場景中的研究內容往往更關注其獨特的三維組裝特徵。
二、干擾素的分子屬性與構象特徵
干擾素作為一類結構敏感度高的小分子蛋白,其氨基酸序列、三維摺疊方式以及分子修飾情況,常被用於描述其分子屬性。I 類干擾素普遍具有較高的序列保守性,其關鍵功能結構域多集中在與受體結合的表面區域。儘管不同亞型的序列存在差異,但整體骨架的 α 螺旋排列方式高度一致。II 類干擾素的關鍵結構域則包括二聚體界面區域,該界面決定了其天然二聚體狀態的穩定性。在 III 類干擾素中,序列差異更多體現在表面可變區,而核心摺疊區域則較為穩定,確保受體識別界面的構象完整。
分子量是討論干擾素結構屬性時的常見指標。I 類干擾素屬於典型的小型細胞因子,其單體結構緊湊,摺疊狀態對温度、pH 和微環境條件較敏感,因此具有較強的構象依賴性。IFN-γ 由於以二聚體形式存在,其整體結構穩定性較高,但二聚界面的完整性仍可能受到環境因素影響。III 類干擾素的分子量略高於 I 類干擾素,但摺疊模式相對清晰,因此在研究中常結合受體結構來解釋其構象特徵。
干擾素蛋白在科研文獻中也常出現“標籤”描述,例如無標籤版本和帶有融合標籤的版本。標籤本身會改變蛋白的空間大小或局部電荷分佈,因此可能對構象穩定性或受體結合界面產生影響。這類影響並不涉及功能討論,而是幫助理解為什麼不同版本的干擾素在實驗記錄中會呈現不同的結構行為。
糖基化是影響干擾素分子屬性的另一個重要因素。IFN-β 在結構上具備天然糖基化位點,因此理論上可能呈現糖基化修飾,使蛋白更穩定或呈現更大的分子量。而大多數 IFN-α 亞型不具備糖基化位點,因此通常以相對“均一”的分子形式出現。IFN-γ 的修飾情況則取決於其表達系統,但理論上糖基化仍可能影響其二聚體結構的空間排列。這樣的結構差異通常在結構研究中被用來討論構象穩定性,而非應用層面的功能表現。
三、干擾素活性與結構完整性的技術理解
在科研技術文獻中,“活性”這一術語常用於描述干擾素在標準化體系中是否保持其天然結構所具備的反應能力。活性並不指任何診斷或治療意義,而是集中於“蛋白是否維持結構完整、是否能與受體形成完整界面”這一純結構學概念。干擾素的活性通常以國際單位(IU)表示,其來源於國際標準品的比對體系。本質上,活性高低反映了蛋白摺疊程度、構象穩定性與受體接觸區域的完整性。
結構與活性之間具有緊密聯繫。對於 I 類干擾素而言,若 α 螺旋束的摺疊發生變化,可能導致其表面與受體結合所需的關鍵氨基酸發生位置偏移,從而影響受體識別效率。對於二聚體結構的 IFN-γ 來説,任何影響二聚界面的因素都可能導致其二聚體解離,從而直接改變其活性相關的結構平台。III 類干擾素的受體結合界面更大,因此其局部構象變化在理論上對活性影響更為顯著。
科研文獻在描述干擾素試劑時,常同時提供序列、分子量、標籤信息和理論活性之間的對應關係,這一做法並非為了強調某種應用,而是便於科研人員理解蛋白結構的完整性。例如,若某版本干擾素帶有標籤,其結構表面可能發生局部改變,從而導致活性值與無標籤版本不一致。在純結構學角度下,這反映了“結構改變 → 活性差異”這一基本規律,而這一規律是科研重複性討論中常見的技術基礎。
對干擾素而言,結構、穩定性、摺疊程度、受體結合幾何關係等因素均可影響其分子表現。科研人員在查閲文獻時,通常會依據這些參數來理解特定實驗體系所採用的蛋白狀態。理解這些結構基礎,有助於在閲讀文獻或進行實驗時,對不同版本干擾素的分子特性形成清晰認識。
參考文獻
1.Thomas, C. et al. Structural basis for receptor recognition by interferons. Nature573, 103–107 (2019).
2.Forni, D., Mantovani, A. & Garlanda, C. Diversity and properties of human type I interferons. Front. Immunol.11, 605673 (2020).
3.Walter, M. R. Structural insights into interferon–receptor interactions. Trends Immunol.36, 1–10 (2019).
4.Broggi, A. et al. Quantitative approaches for interferon measurement. J. Exp. Med.214, 1547–1560 (2017).
5.Kotenko, S. V. & Durbin, J. E. Functional architecture of type I interferons. Nat. Rev. Immunol.19, 84–96 (2018).
6.Crow, Y. J. & Stetson, D. B. Interferon signaling and regulation. Nat. Rev. Immunol.21, 1–15 (2021).
7.Comi, M. et al. Transcriptional programs linked to interferon responses. Nat. Immunol.23, 632–642 (2022).
8.Garcia, K. C. et al. Mechanisms of interferon receptor engagement. Structure26, 1–12 (2018).