一、項目背景:無菌注射劑灌裝生產線的通訊困境
在工業自動化領域的醫藥無菌注射劑灌裝生產線中,某企業採用施耐德 HMI(Modbus RTU 協議)負責灌裝參數設定(如劑量 5ml±0.02ml)、設備操作監控,搭配西門子 S7-1500 PLC(Modbus TCP 協議)控制灌裝閥、無菌隔離艙、在線檢漏設備的運行。
兩者需實時協同:HMI 需向 S7-1500 PLC 下發灌裝劑量、灌裝速度(100 瓶 / 分鐘)、無菌艙壓力設定值(0.12MPa),S7-1500 PLC 需反饋實際灌裝劑量、設備運行狀態、檢漏結果(合格 / 不合格),以保障注射劑劑量精度與無菌安全。但因雙方採用不同總線協議,缺乏直接通訊通道,原有 “操作員在 HMI 記錄參數後手動錄入 PLC” 的銜接方式效率低下,日均因參數偏差導致的生產停滯達 2 次,單次停滯需廢棄整批藥液(約 2000 瓶),直接損失超 12 萬元。無菌注射劑生產作為醫藥行業的核心領域,是工業自動化中對無菌控制、劑量精度要求極高的前景行業(2025 年全球注射劑市場規模預計超 1800 億美元),對工業物聯網環境下數據的實時性、合規性提出了嚴苛標準(符合 GMP、FDA 21 CFR Part 11 要求)。
二、項目痛點
1. 協議異構阻斷灌裝控制:HMI 的 Modbus RTU 協議與 S7-1500 PLC 的 Modbus TCP 協議無法直接兼容,無物聯網網關中轉時,灌裝參數需操作員每 15 分鐘在 HMI 記錄後,通過 PLC 編程軟件手動輸入,單次數據傳遞延遲超 20 分鐘,導致灌裝劑量控制偏差超 0.05ml,曾引發 1 批註射劑劑量不合格,報廢損失超 15 萬元;生產節拍從 100 瓶 / 分鐘降至 60 瓶 / 分鐘,日產能從 12 萬瓶降至 7.2 萬瓶,效率下降 40%。
2. 數據採集追溯斷層:原有系統無專用數據採集器,灌裝劑量、無菌艙壓力、檢漏合格率等關鍵工藝數據僅分別存儲於 HMI 本地(存儲週期 24 小時)與 PLC 內存,無法自動上傳至工業物聯網平台與 GMP 數據歸檔系統,審計追蹤時需人工整理紙質記錄,耗時超 60 小時,不符合 FDA 21 CFR Part 11 對 “電子數據不可篡改、可追溯” 的要求,面臨監管部門整改風險。
3. 工業環境適應性差:生產線位於無菌潔淨區(Class 100),傳統 RS485 轉以太網模塊防護等級低(IP20)、不耐受潔淨區的濕熱滅菌(温度 121℃、濕度 100%),日均通訊中斷 1-2 次,每次中斷需停產消毒並重啓設備,恢復耗時超 4 小時,單日減少有效生產時間約 8 小時,損失產能超 4.8 萬瓶。
4. 設備負載超限引發安全風險:嘗試通過第三方軟件實現數據轉發,導致 HMI 觸控響應延遲超 3 秒(CPU 負載升至 89%)、S7-1500 PLC CPU 負載達 85%,超出安全運行閾值(HMI≤80%、PLC≤75%),引發灌裝閥開關延遲,導致部分瓶體漏液,漏液率從 0.1% 升至 0.8%,額外增加清潔與物料損失成本超 6 萬元 / 月。
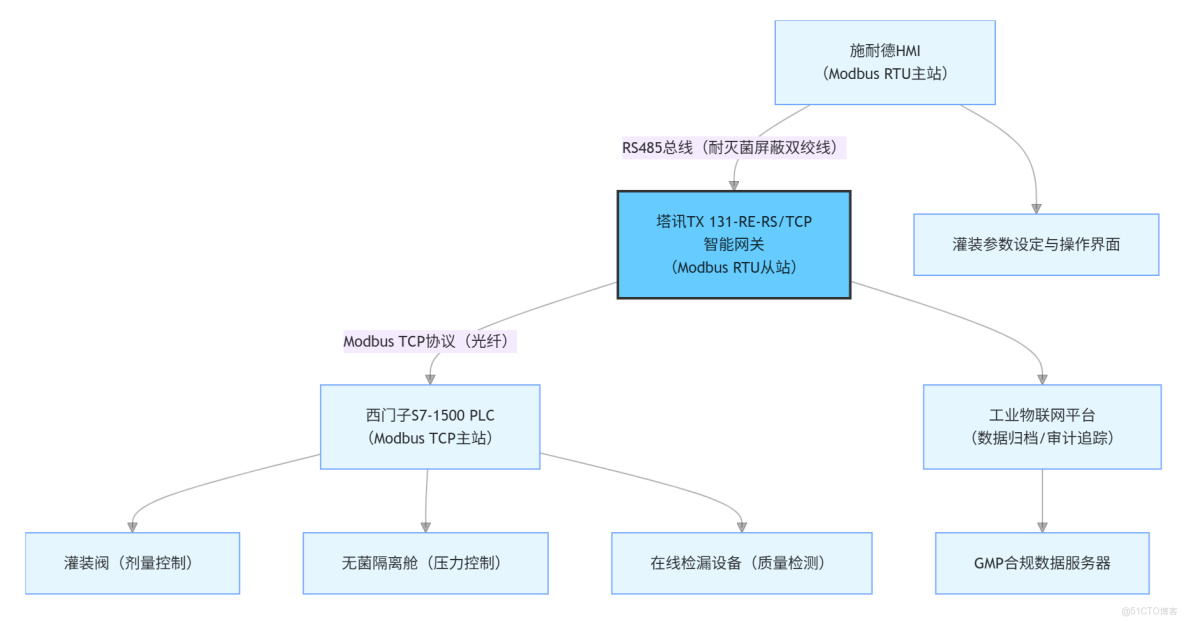
三、系統結構拓撲圖
四、塔訊 TX 131-RE-RS/TCP 網關功能簡介
作為核心工業網關,該設備實現 Modbus RTU 從站到 Modbus TCP 從站的雙向協議轉換,關鍵功能深度適配無菌注射劑灌裝場景需求:
· 協議兼容:嚴格遵循 Modbus RTU(IEC 61158)與 Modbus TCP(IEC 61158)協議規範,支持 9600-115200bps 可調波特率(適配 HMI 通訊參數:9600bps、偶校驗、8 數據位、1 停止位)與 10/100Mbps 自適應以太網速率,自動識別 S7-1500 PLC 的寄存器地址映射規則,確保灌裝參數與指令傳輸無格式偏差,符合注射劑 “劑量零誤差” 要求。
· 數據處理:內置雙核工業級處理器,每秒可完成 2300 次以上數據轉換,轉換延遲≤21μs,支持 1800 點數據映射,滿足灌裝劑量(4 字節浮點數)、無菌艙壓力(4 字節浮點數)、檢漏結果(1 字節布爾值)等多類型數據同步傳輸,數據更新頻率達 2 次 / 秒,符合 GMP 對 “實時監控” 的標準。
· 工業適配:具備 IP40 防護等級(適配潔淨區環境),外殼採用 316L 不鏽鋼材質(耐濕熱滅菌、耐腐蝕),支持 24VDC 寬壓供電(±10% 波動兼容);採用寬温設計(10℃-50℃),耐受潔淨區温濕度波動;抗電磁干擾性能符合 EN 61000-6-2 標準,避免檢漏設備高頻信號導致的數據丟包。
· 物聯與合規擴展:支持本地數據緩存(容量 3GB,緩存週期 90 天),通過 MQTT 協議對接工業物聯網平台與 GMP 數據服務器,實現工藝數據實時歸檔與不可篡改存儲;內置審計追蹤日誌功能,記錄每一次參數修改、數據傳輸的時間戳與操作員信息,滿足 FDA 21 CFR Part 11 要求;支持故障自恢復,通訊中斷後≤80ms 重新建立連接,保障無菌生產連續。
五、解決方案與實施過程
(一)方案設計
採用塔訊智能網關構建 “HMI - 網關 - PLC” 通訊架構:網關 Modbus RTU 側作為 HMI 的從站,實時採集灌裝劑量(DB1.DBD10)、灌裝速度(DB1.DBD20)、無菌艙壓力設定值(DB1.DBD30);Modbus TCP 側作為 S7-1500 PLC 的從站,將採集到的參數傳輸至 PLC,同時接收 PLC 反饋的實際劑量(DB2.DBD10)、設備狀態(M10.0-M10.2)、檢漏結果(DB2.DBD20),實現雙向數據實時交互,數據更新頻率 2 次 / 秒,滿足注射劑灌裝控制需求。
(二)實施步驟
1. 硬件部署:網關安裝於潔淨區外的控制室機櫃內,通過耐滅菌屏蔽 RS485 電纜(長度 30 米,穿牆接線盒密封處理)接入 HMI 的 RS485 通訊端口;通過單模光纖(抗干擾性強,適配潔淨區與控制室 400 米距離)連接 S7-1500 PLC 的以太網交換機,配置 IP 地址(192.168.11.100)與 PLC(192.168.11.10)同網段,做好獨立接地處理(接地電阻≤4Ω),避免車間靜電干擾。
2. 參數配置:使用塔訊配置軟件建立數據映射表 —— 將 HMI 的灌裝參數(劑量:40001、速度:40002、壓力:40003)映射至網關寄存器;將 PLC 的反饋數據(實際劑量:30001、設備狀態:10001-10003、檢漏結果:30002)映射至網關對應寄存器,設置數據更新週期 100ms,啓用 “數據校驗”“審計日誌”“斷網重連” 功能,日誌保存週期 90 天。
3. 聯調與合規測試:在工業物聯網平台與 HMI 同步驗證數據傳輸(延遲≤21μs,丟包率 0%);模擬灌裝劑量調整(從 5ml 降至 2ml),測試 PLC 接收指令後灌裝閥的響應時間(≤50ms);邀請第三方機構驗證審計日誌符合 FDA 21 CFR Part 11 要求,確保通過 GMP 複評。
六、應用效果與前後對比
(一)實施後效果
1. 灌裝精度與合規性雙提升:數據傳輸延遲降至 21μs 內,HMI 與 PLC 參數同步無偏差,灌裝劑量控制偏差從 ±0.05ml 降至 ±0.01ml,劑量不合格事件從 2 次 / 日降至 0 次,每月減少產品廢棄損失超 36 萬元;生產節拍從 60 瓶 / 分鐘提升至 110 瓶 / 分鐘,日產能從 7.2 萬瓶增至 13.2 萬瓶,效率提升 83%,滿足市場對注射劑的激增需求。
2. 數據追溯效率大幅提升:通過網關將工藝數據自動歸檔至工業物聯網平台與 GMP 服務器,審計追蹤時間從 60 小時縮短至 12 分鐘,順利通過 FDA 現場檢查;數據不可篡改功能保障電子數據合規,未再出現監管整改風險。
3. 通訊穩定性適配潔淨區環境:網關 IP40 防護與耐滅菌設計適配潔淨區工況,連續運行 3 個月無通訊中斷,設備故障率從 9% 降至 0.3%,停產恢復時間從 4 小時縮短至 15 分鐘,單日增加有效生產時間 8 小時,月增產能超 38.4 萬瓶。
4. 設備負載與安全風險降低:HMI 觸控響應延遲從 3 秒降至 0.1 秒(CPU 負載從 89% 降至 41%),S7-1500 PLC CPU 負載從 85% 降至 37%,均低於安全閾值;灌裝閥開關延遲消除,漏液率從 0.8% 降至 0.05%,每年減少清潔與物料損失成本超 72 萬元。
(二)效果對比表
|
指標 |
實施前 |
實施後 |
|
數據傳輸延遲 |
>20 分鐘 |
≤21μs |
|
灌裝劑量偏差 |
±0.05ml |
±0.01ml |
|
設備丟包率 |
>6% |
0% |
|
HMI CPU 負載 |
89% |
41% |
|
PLC CPU 負載(S7-1500) |
85% |
37% |
|
審計追蹤時間 |
>60 小時 |
<12 分鐘 |
|
日均通訊中斷次數 |
1-2 次 |
0 次 |
七、行業價值與後續擴展
本案例聚焦無菌注射劑灌裝行業,該行業關乎患者用藥安全,對生產過程的精度與合規性要求極高。此方案可複製至疫苗灌裝、生物製劑灌裝等場景,後續可擴展接入 MES 系統,實現灌裝數據與生產訂單、質量檢測數據聯動;或對接 AI 視覺檢測系統,通過工業物聯網平台分析灌裝瓶體外觀數據,自動識別瑕疵品,進一步提升注射劑生產的安全性與效率,助力企業滿足全球嚴苛的醫藥監管標準。